loading...
(Thethaovanhoa.vn) - Bộ Y tế vừa ban hành Quyết định số 2763/QĐ-BYT về việc phê duyệt có điều kiện vaccine cho nhu cầu cấp bách trong phòng, chống dịch COVID-19.

Chiều 3/6, tại Họp báo Chính phủ thường kỳ tháng 5, trao đổi về vấn đề cơ chế cho doanh nghiệp, tổ chức, cá nhân tham gia mua vacine và cơ chế kiểm soát chất lượng vaccine.
Theo Quyết định, Bộ Y tế phê duyệt có điều kiện vaccine cho nhu cầu cấp bách trong phòng, chống dịch COVID-19 theo quy định tại Điều 67 Nghị định số 54/2017/NĐ-CP ngày 8/5/2017 của Chính phủ quy định chi tiết một số điều và biện pháp thi hành Luật dược (Nghị định 54/2017/NĐ-CP).
Cụ thể, tên vaccine là COVID-19 Vaccine (Vero Cell), Inactivated (tên khác là SARS- CoV-2 Vaccine (Vero Cell), Inactivate). Thành phần hoạt chất, nồng độ/hàm lượng: Mỗi liều 0,5ml chứa 6.5U kháng nguyên SARS-CoV-2 bất hoạt.
Dạng bào chế: Hỗn dịch tiêm. Quy cách đóng gói: Hộp 1 lọ, 3 lọ; mỗi lọ chứa 1 liều 0,5ml. Hộp 1 bơm tiêm chứa 1 liều 0,5m.
Cơ sở sản xuất - Nước sản xuất là: Beijing Institute of Biological Products Co., Ltd. - Trung Quốc. Tên cơ sở đề nghị phê duyệt vaccine là Viện Vệ sinh dịch tễ Trung ương.
Theo Quyết định, Cục Quản lý Dược có trách nhiệm cấp phép nhập khẩu vaccine COVID-19 Vaccine (Vero Cell), Inactivated theo quy định tại Điều 67 Nghị định 54/2017/NĐ-CP khi nhận được hồ sơ của cơ sở nhập khẩu; thực hiện đúng quy định của pháp luật về quản lý nhập khẩu, quản lý chất lượng vaccine nhập khẩu.
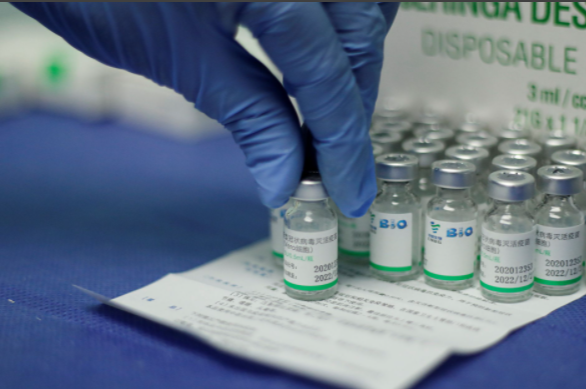 Vắc xin ngừa COVID-19 của Hãng Sinopharm, Trung Quốc. Ảnh: REUTERS
Vắc xin ngừa COVID-19 của Hãng Sinopharm, Trung Quốc. Ảnh: REUTERS
Cục Khoa học công nghệ và Đào tạo có trách nhiệm lựa chọn đơn vị có đủ điều kiện đánh giá tính an toàn, hiệu quả của vaccine trên cơ sở ý kiến tư vấn của Hội đồng tư vấn sử dụng vaccine, sinh phẩm y tế của Bộ Y tế trong quá trình sử dụng; hướng dẫn, chỉ đạo đơn vị có đủ điều kiện quy định tổ chức thực hiện việc đánh giá tính an toàn; hiệu quả của vaccine COVID-19 Vaccine (Vero Cell), Inactivated trên cơ sở ý kiến tư vấn của Hội đồng tư vấn sử dụng vaccine, sinh phẩm y tế của Bộ Y tế trong quá trình sử dụng.
Cục Y tế Dự phòng thực hiện các trách nhiệm liên quan đến tiêm chủng vaccine COVID-19 Vaccine (Vero Cell), Inactivated được quy định tại Quyết định số 1464/QĐ-BYT ngày 5/3/2021 của Bộ trưởng Bộ Y tế về việc ban hành hướng dẫn tiếp nhận, bảo quản, phân phối và sử dụng vaccine phòng COVID-19 và Quyết định số 1467/QĐ-BYT ngày 5/3/2021 của Bộ trưởng Bộ Y tế về việc phê duyệt kế hoạch tiêm vaccine phòng COVID-19 giai đoạn 2021 - 2022.
Viện Kiểm định Quốc gia vaccine và sinh phẩm y tế có trách nhiệm tiến hành kiểm định vaccine COVID-19 Vaccine (Vero Cell), Inactivated trước khi đưa ra sử dụng.
Các điều kiện đi kèm việc phê duyệt vaccine COVID-19 Vaccine (Vero Cell), Inactivated cho nhu cầu cấp bách trong giai đoạn phòng, chống dịch COVID-19 được Bộ Y tế đưa ra là:
Vaccine COVID-19 Vaccine (Vero Cell), Inactivated được phê duyệt dựa trên dữ liệu an toàn, chất lượng và hiệu quả do Viện Vệ sinh dịch tễ Trung ương cung cấp cho Bộ Y tế Việt Nam tính đến ngày 29/5/2021 và cam kết của Viện Vệ sinh dịch tễ Trung ương về tính chính xác của các tài liệu đã cung cấp cho Bộ Y tế Việt Nam.
Viện Vệ sinh dịch tễ Trung ương có trách nhiệm phối hợp với cơ sở sản xuất vaccine phản hồi kịp thời các yêu cầu từ Bộ Y tế Việt Nam để bổ sung thêm dữ liệu hoặc các yêu cầu khác có liên quan đến vaccine COVID-19 Vaccine (Vero Cell), Inactivated và chủ động cung cấp, cập nhật các thông tin mới có liên quan đến vaccine COVID-19 Vaccine (Vero Cell), Inactivated cho Bộ Y tế Việt Nam trong suốt quá trình phát triển sản phẩm.
Đồng thời, Viện có trách nhiệm phối hợp với cơ sở sản xuất vaccine đảm bảo các điều kiện sản xuất vaccine COVID-19 Vaccine (Vero Cell), Inactivated nhập khẩu vào Việt Nam và đảm bảo an toàn, hiệu quả, chất lượng của lô vaccine COVID-19 Vaccine (Vero Cell), Inactivated nhập khẩu vào Việt Nam.
Viện Vệ sinh dịch tễ Trung ương triển khai hệ thống cảnh giác dược toàn diện đối với vaccine COVID-19 Vaccine (Vero Cell), Inactivated tại Việt Nam theo quy định của pháp luật.
Bên cạnh đó, Viện Vệ sinh dịch tễ Trung ương phải phối hợp với Cục Khoa học công nghệ và Đào tạo và đơn vị có đủ điều kiện tổ chức thực hiện việc đánh giá tính an toàn và hiệu quả của vaccine COVID-19 Vaccine (Vero Cell), Inactivated trên cơ sở ý kiến tư vấn của Hội đồng tư vấn sử dụng vaccine, sinh phẩm y tế của Bộ Y tế trong quá trình sử dụng.
Viện Vệ sinh dịch tễ Trung ương phải phối hợp với Viện Kiểm định Quốc gia vaccine và sinh phẩm y tế về xây dựng kế hoạch kiểm định; cung cấp mẫu thử, nguyên vật liệu, hóa chất thử nghiệm và các vấn đề liên quan khác cho việc kiểm định các lô vaccine COVID-19 Vaccine (Vero Cell), Inactivated trước khi đưa ra sử dụng.
Viện Vệ sinh dịch tễ Trung ương hướng dẫn việc bảo quản, phân phối và sử dụng vaccine COVID-19 Vaccine (Vero Cell), Inactivated cho các cơ sở tiêm chủng; phối hợp với các đơn vị liên quan để triển khai quản trị rủi ro đối với vaccine COVID-19 Vaccine (Vero Cell), Inactivated trong suốt quá trình lưu hành tại Việt Nam.
Việc sử dụng vaccine COVID-19 Vaccine (Vero Cell), Inactivated phải theo hướng dẫn của Bộ Y tế Việt Nam.
TTXVN
loading...