Thông tin rõ hơn về vaccine Nanocovax từ phía đơn vị nghiên cứu thử nghiệm
(Thethaovanhoa.vn) - Học viện Quân y - đơn vị tham gia nghiên cứu thử nghiệm vaccine Nanocovax do Công ty cổ phần Công nghệ sinh học dược Nanogen đăng ký và sản xuất, khẳng định đã thực hiện các xét nghiệm quan trọng để đánh giá tính sinh miễn dịch của sản phẩm và tin tưởng sau khi vaccine này được cấp phép Việt Nam sẽ chủ động hơn về “vũ khí” trong chống dịch COVID-19.
Đây là khẳng định của Thiếu tướng, Phó Giáo sư, Tiến sỹ Nguyễn Viết Lượng, Chính ủy Học viện Quân y, Bộ Quốc phòng - đơn vị tham gia nghiên cứu thử nghiệm trong cuộc phỏng vấn với TTXVN gần đây.
Trước đó, ngày 29/8/2021, sau khi họp xem xét hồ sơ đề nghị cấp Giấy đăng ký lưu hành vaccine Nanocovax phòng COVID-19 do Công ty cổ phần Công nghệ sinh học dược Nanogen đăng ký và sản xuất, Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc (Hội đồng tư vấn), Bộ Y tế, ghi nhận những kết quả đạt được đối với hồ sơ đề nghị, đã được các tiểu ban thẩm định, Hội đồng Đạo đức trong nghiên cứu y sinh học quốc gia (Hội đồng Đạo đức) nghiệm thu.
Đồng thời đề nghị doanh nghiệp khẩn trương bổ sung, cập nhật một số nội dung về hồ sơ chất lượng; dữ liệu an toàn về hồ sơ dược lý, lâm sàng; tính sinh miễn dịch trên các biến chủng mới và cỡ mẫu đánh giá tính sinh miễn dịch theo đúng đề cương nghiên cứu đã được thông qua; về mối liên hệ giữa tính sinh miễn dịch của vaccine và hiệu quả bảo vệ tối thiểu 50% theo hướng dẫn của Tổ chức Y tế Thế giới dựa trên các dữ liệu y văn.
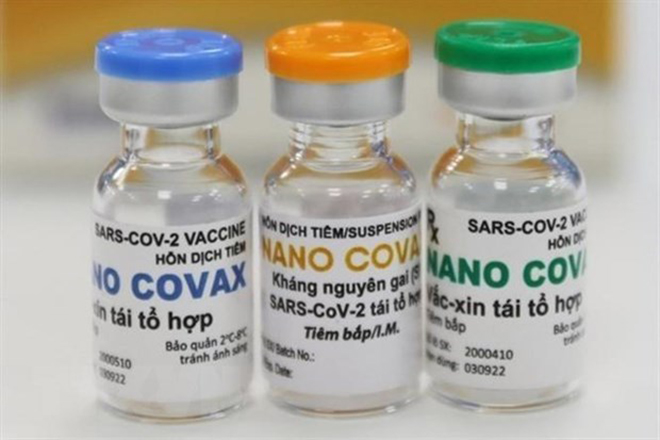
Hội đồng tư vấn cũng yêu cầu Nagogen khẩn trương bổ sung, cập nhật các yêu cầu trên để báo cáo Hội đồng Đạo đức và Hội đồng tư vấn tiếp tục xem xét, thẩm định cuốn chiếu các kết quả nghiên cứu để có thể cấp giấy đăng ký lưu hành có điều kiện trong trường hợp cấp bách.
Trong cuộc trao đổi, Phó Giáo sư, Tiến sỹ Nguyễn Viết Lượng đề cập sâu về 4 xét nghiệm quan trọng để đánh giá tính sinh miễn dịch của Nanocovax, một trong các nội dung Hội đồng tư vấn yêu cầu bổ sung và cập nhật thông tin.
Phó Giáo sư, Tiến sỹ Nguyễn Viết Lượng cho biết, tính sinh miễn dịch (bằng xét nghiệm định lượng kháng thể IgG kháng SARS-CoV-2) của vaccine Nanocovax đạt 57,56 U/ml.
Phó Giáo sư, Tiến sỹ Nguyễn Viết Lượng cho rằng, để so sánh nồng độ kháng thể IgG của các loại vaccine đều phải thực hiện trên cùng một đơn vị đo (đơn vị chuẩn của WHO là BAU/ml). Thậm chí, để bảo đảm tính chính xác khi so sánh, các vaccine phải sử dụng cùng một loại kit xét nghiệm, trong khi ở đây các nghiên cứu sử dụng các loại kit khác nhau với các đơn vị đo khác nhau.
“Để đánh giá tính sinh miễn dịch của vaccine phải dựa vào nhiều tiêu chí khác, không chỉ dựa vào nồng độ kháng thể IgG”, Phó Giáo sư, Tiến sỹ Nguyễn Viết Lượng nhấn mạnh.
- Bộ Y tế thông tin về mở rộng địa điểm tiêm thử nghiệm giai đoạn 3 vaccine Nanocovax
- Nghiên cứu giảm thủ tục cấp phép cho vaccine Nanocovax phòng Covid-19
- Thủ tướng chỉ đạo về việc cấp phép và sử dụng vaccine Nanocovax
Theo đó, trong nghiên cứu vaccine Nanocovax, các đơn vị đã sử dụng 4 xét nghiệm để đánh giá, bao gồm: Xét nghiệm định lượng kháng thể; đánh giá kháng thể trung hòa (surrogate neutralization antibody); đánh giá kháng thể trung hòa trên virus sống bằng phương pháp PRNT (plaque reduction neutralization test); đánh giá miễn dịch qua trung gian tế bào. Trong đó, ngoài xét nghiệm định lượng kháng thể, đánh giá kháng thể trung hòa và đánh giá kháng thể trung hòa trên virus sống bằng PRNT được xem là các tiêu chí quan trọng.
Thông tin thêm về hiệu quả sinh miễn dịch của vaccine Nanocovax, Phó Giáo sư, Tiến sỹ Nguyễn Viết Lượng cho biết, để chuẩn hóa số liệu, nhiều nghiên cứu vaccine sử dụng phương pháp so sánh với huyết thanh của người mắc COVID-19 đã khỏi bệnh. Ở nghiên cứu này, kết quả cho thấy, hiệu quả kháng thể IgG của tất cả các mẫu huyết thanh nghiên cứu ở bệnh nhân mắc COVID-19 đã hồi phục trung bình đạt 5,63 U/ml. Trong khi đó, IgG của nhóm tình nguyện viên tiêm vaccine Nanocovax (ở liều tiêm 25 mg) ngày thứ 35 đạt 6,77 U/ml, ở ngày thứ 42 đạt 60,47 U/ml, đến ngày 90 đạt 16,25 U/ml.
Mặc dù, tại ngày thứ 90 sau tiêm, hàm lượng kháng thể anti-S IgG ở các tình nguyện viên tiêm vaccine giảm đi 3,7 lần so với ngày thứ 42 (từ mức 60,47 U/ml xuống 16,25 U/ml) nhưng vẫn cao hơn nhóm bệnh nhân mắc COVID-19 đã hồi phục gần 2,9 lần (16,25 U/ml so với 5,63 U/ml).
Phó Giáo sư, Tiến sỹ Nguyễn Viết Lượng cho biết thêm, ngoài ra, nếu so sánh với các con số được công bố của vaccine Moderna về mức tăng nồng độ kháng thể của nhóm tiêm vaccine với nhóm bệnh nhân mắc COVID-19 đã hồi phục, tại thời điểm đạt đỉnh (ngày thứ 42 sau tiêm), vaccine Moderna có mức tăng 5,19 lần còn vaccine Nanocovax có mức tăng 10,74 lần (60,47 U/ml so với 5,63 U/ml).
Đối với khả năng trung hòa surrogate neutralization, kết quả nghiên cứu trên Nanocovax cũng cho thấy, tỷ lệ trung hòa của các mẫu huyết thanh trên bệnh nhân mắc COVID-19 đã hồi phục đạt 5,68% trong khi đó ở nhóm tình nguyện viên sau khi tiêm vaccine Nanocovax (liều 25 mg) ngày thứ 35 đạt 58,39%, ngày thứ 42 đạt 85,5% và ngày thứ 90 đạt 72,68%.
Ở nhóm tiêm vaccine Nanocovax liều 25 mg, tại ngày thứ 90 sau tiêm kết quả đã giảm so với ngày thứ 42 (1,17 lần) nhưng mức giảm vẫn thấp hơn nhóm bệnh nhân mắc COVID-19 đã hồi phục (nhóm này giảm 1,27 lần).
Về sự suy giảm nồng độ kháng thể sau mức đạt đỉnh của vaccine, Thiếu tướng Nguyễn Viết Lượng giải thích, thông thường thời gian bán hủy của IgG khoảng 25 ngày, có nghĩa, tất cả các loại vaccine sau khi kích thích cơ thể tạo ra kháng thể IgG đạt đỉnh, nồng độ kháng thể đều suy giảm dần. “Như vậy, không có nghĩa vaccine mất đi khả năng bảo vệ. Việc tiêm vaccine giúp cơ thể hình thành nên các tế bào B đặc hiệu. Tế bào này sẽ tiếp tục sản xuất ra kháng thể khi có kháng nguyên hoặc virus xâm nhập. Điều này cũng cho thấy, việc tiêm nhắc lại vaccine phòng COVID-19 sau một khoảng thời gian nhất định là cần thiết”, Thiếu tướng Nguyễn Viết Lượng chia sẻ.
Nêu dẫn chứng về mức độ giảm kháng thể của vaccine đã được cấp phép khẩn cấp Moderna, Phó Giáo sư, Tiến sỹ Nguyễn Viết Lượng cho biết, theo kết quả nghiên cứu được Moderna công bố, ngày thứ 119 so với ngày thứ 43 sau tiêm, nồng độ kháng thể giảm 3,96 lần; tương đương với mức giảm của Nanocovax 3,7 lần (16,25 U/ml ở ngày thứ 90 so với 60,47 U/ml ở ngày thứ 42).
Mặc dù nồng độ kháng thể ngày 90 giảm so với ngày 42 nhưng so sánh với nhóm bệnh nhân mắc COVID-19 đã hồi phục, mức kháng thể đạt được ở ngày 90 của nhóm tiêm vaccine vẫn cao hơn nhiều so với nhóm bệnh nhân mắc COVID-19 đã hồi phục (16,25 U/ml so với 5,63 U/ml).

* Về hai trường hợp theo dõi phản vệ trong quá trình thử nghiệm
Phó Giáo sư, Tiến sỹ Nguyễn Viết Lượng cho biết, trong nghiên cứu thử nghiệm lâm sàng vaccine Nanocovax có 2 trường hợp theo dõi phản vệ (phản vệ độ 1 và phản vệ độ 2) và không có trường hợp phản vệ độ 3 (hay còn gọi là “sốc phản vệ”) trong cả 3 giai đoạn nghiên cứu. Hai trường hợp này đều đã được xử trí kịp thời theo phác đồ của Bộ Y tế, sau đó đã hồi phục sức khỏe, trở về trạng thái hoàn toàn bình thường. Học viện Quân y cũng đã báo cáo Hội đồng đạo đức cấp cơ sở, Cục Khoa học Công nghệ và Đào tạo (Bộ Y tế), Hội đồng Đạo đức trong nghiên cứu Y sinh học Quốc gia, Trung tâm Quốc gia về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc, theo đúng quy định.
“2/13.627 tình nguyện viên phản vệ không phải là tỷ lệ lớn so với công bố của nhiều loại vaccine khác. Hơn nữa, đây chỉ là phản vệ độ 1, độ 2, chưa đến mức nghiêm trọng cần phải “mở mù” nghiên cứu,” Phó Giáo sư, Tiến sỹ Nguyễn Viết Lượng nhấn mạnh.
* Quy trình bảo mật và minh bạch thông tin nghiên cứu
Theo Phó Giáo sư, Tiến sỹ Nguyễn Viết Lượng, khi ứng viên vaccine chưa được Hội đồng cấp phép thông qua chính thức, mọi số liệu về kết quả nghiên cứu được nhà sản xuất và các tổ chức tham gia nghiên cứu đánh giá trình Hội đồng Đạo đức của Bộ Y tế đều được xem là tài liệu chưa được phép công bố, trừ những bài báo khoa học liên quan do nhà sản xuất hoặc các tổ chức nghiên cứu đánh giá thử nghiệm công bố. Quy định này nhằm bảo vệ quyền lợi chính đáng cho nhà sản xuất và các cơ quan tham gia nghiên cứu đánh giá cũng như bảo đảm các cam kết về vấn đề đạo đức trong nghiên cứu.
“Việc công bố các số liệu về kết quả nghiên cứu phải được sự đồng ý của nhà sản xuất và các cơ quan nghiên cứu, đánh giá. Do đó, ngay cả những thông tin về một số kết quả nghiên cứu nêu trên cũng phải được sự đồng ý từ phía Nanogen và các nhóm nghiên cứu đánh giá thử nghiệm vaccine Nanocovax”, Phó Giáo sư, Tiến sỹ Nguyễn Viết Lượng cho biết.
Ông cũng chia sẻ thêm, những thông tin sai lệch, thiếu căn cứ không chỉ gây hoang mang dư luận mà còn ảnh hưởng trực tiếp đến các tình nguyện viên cũng như nhà sản xuất, đơn vị, tổ chức, những người làm khoa học tham gia nghiên cứu.
* Hy vọng thêm một “vũ khí quan trọng” trong cuộc chiến phòng, chống dịch COVID-19
Phó Giáo sư, Tiến sỹ Nguyễn Viết Lượng cho biết thêm, sau khi xem xét báo cáo về kết quả nghiên cứu đánh giá giai đoạn 1, giai đoạn 2 và giữa kỳ giai đoạn 3 (giai đoạn 3a) của vaccine Nanocovax, Hội đồng Đạo đức đã có biên bản kết luận và chuyển hồ sơ sang Hội đồng tư vấn xem xét cấp phép khẩn cấp có điều kiện cho vaccine Nanocovax.
“Những đánh giá, nhận xét của Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia là đúng mực, công bằng, khách quan. Hiện nay, doanh nghiệp và các đơn vị tham gia nghiên cứu đã bổ sung các hồ sơ theo yêu cầu tại cuộc họp xem xét hồ sơ đề nghị cấp Giấy đăng ký lưu hành vaccine Nanocovax phòng COVID-19 ngày 29/8. Hy vọng vaccine Nanocovax sẽ sớm được Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc, cấp phép khẩn cấp trong nửa đầu tháng 9/2021 để Việt Nam có thêm một “vũ khí quan trọng” trong cuộc chiến phòng, chống dịch, góp phần bảo vệ sức khỏe, tính mạng của nhân dân, sớm đưa cuộc sống trở về trạng thái bình thường mới”, Phó Giáo sư, Tiến sỹ Nguyễn Viết Lượng chia sẻ.
Diệp Trương - TTXVN